胰高血糖素是高血糖的必要条件
糖尿病(diabetes mellitus,DM)是由多种因素(包括遗传、免疫功能紊乱及精神因素等)导致的胰岛功能减退或胰岛素抵抗(IR)进而引起糖、蛋白质、脂肪等代谢异常 [1] 。
为什么高额医疗支出依然无法阻挡患者的猛增?
全球糖尿病患者激增,由1980年的1.08亿人增加到2015年的4.15亿人,糖尿病医疗保健支出总额达6730亿美元,占全球医疗费用的12%。全球糖尿病药物市场约600亿美元,位居世界第二大药物种类。我国糖尿病患者高达1.1亿人,目前糖尿病用药市场规模预计在213亿元(人民币),由于存在发病率高、诊断率及治疗率低、控制率低、合并并发症机率高的特点,市场潜在空间巨大。
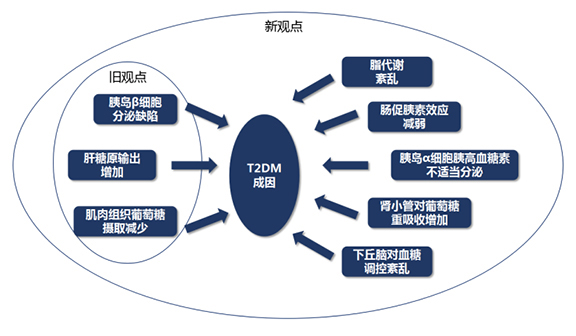
关于2型糖尿病的成因,已从过去的“三英会”扩展到“八重奏” [2] 。
胰岛孔窗结构
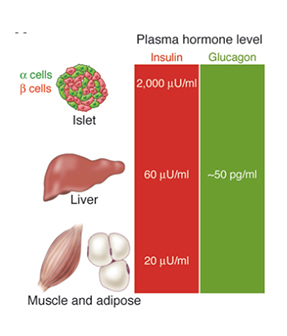
胰岛能够迅速感知体内代谢环境的变化,通过分泌各种激素,调节机体代谢平衡。胰岛内分泌细胞主要包括α细胞、β细胞,分别产生胰高血糖素(Glucagon)、胰岛素。胰岛β细胞位于胰岛中央,α细胞包绕在β细胞周围,二者之间存在间隙连接,细胞内的小分子可不经过细胞膜直接从一种细胞转运另外一种细胞而相互作用 [3] 。

解剖证据揭示,在胰岛素到达体内其他受体之前,胰岛素就通过旁分泌途径到达α细胞,并且浓度远高于输送到外周组织胰岛素受体的浓度水平 [4-6] 。
胰岛素和胰高血糖素拮抗关系
胰岛素与胰高血糖素对肝脏的应答是直接地拮抗作用 [7] ,表明这两种激素共同负责调节肝糖代谢。通过用生长抑素来抑制血液中胰高血糖素和胰岛素一直处于基础水平的研究证实了胰高血糖素刺激体内生成葡萄糖的作用 [8] 。
胰高血糖素迅猛应答
维持过夜禁食后的血糖正常水平,七成以上由胰高血糖素应答产生 [9] ;而且,血浆中胰高血糖素仅需升高100pg/mL就能促使肝糖原分解出空腹时血糖的三倍量 [10,11] 。所以需要对胰高血糖素进行严格的监控,在血浆中胰高血糖素浓度的生理动态变化范围5mg/kg/min [12-17] 。肝脏不仅对胰高血糖素浓度的变化非常敏感,而且应答迅速,多数仅需8分钟即可被刺激应答 [18] 。
高水平的胰高血糖素是绝大部分糖尿病患者均会出现高血糖的必要条件
血糖波动不稳定,患者必须不间断地监测血糖水平;补充胰岛素或口服葡萄糖来应对和纠正高血糖或低血糖的情况是最具挑战性的日常临床问题 [19-21] 。
无论是胰岛素绝对缺陷的T1DM还是相对缺陷的T2DM,都无法有效纠正高胰高血糖素血症造成的肝糖输出增加和血糖水平升高 [22] 。
T2DM患者胰岛β细胞的分泌功能随时间延长呈进行性减退,从而导致其对胰高血糖素抑制减弱,胰高血糖素含量升高及胰岛β细胞功能受损加剧了餐后高血糖 [23] 。
为了满足所有组织的需要只能注射相同高水平浓度的胰岛素,这导致了α细胞需要胰岛素的量不足而外周组织胰岛素的量过多,最严重时出现低血糖昏迷 [19-21] 。
参考文献:
【1】李影,张真稳.线粒体损伤与糖尿病发病的相关机制.国际内分泌代谢杂志,2014,34:271-273,280.
【2】刘玥明,闻杰,李益明,中国糖尿病患者胰岛功能的困境与出路,药品评价 2016年第13卷第7期.
【3】谷丽,张丽,胰岛α细胞在糖尿病发病及治疗领域中的研究进展,中国糖尿病杂志2017年2月第25卷第2期.
【4】Bonner-Weir S, Orci L. New perspectives on the microvasculature of the islets of Langerhans in the rat. Diabetes. 1982;31(10):883–889.
【5】Bosco D, et al. Unique arrangement of alpha- and beta-cells in human islets of Langerhans. Diabetes. 2010;59(5):1202–1210.
【6】Meda P, Kohen E, Kohen C, Orci L. [Heterocellular coupling in cultures of endocrine pancreatic cells]. C R Seances Acad Sci III. 1981;293(10):607–610.
【7】Cherrington A, Vranic M. Role of glucagon and insulin in control of glucose turnover. Metabolism. 1971; 20(6):625–628.
【8】Cherrington AD, Liljenquist JE, Shulman GI, Williams PE, Lacy WW. Importance of hypoglycemia- induced glucose production during isolated glucagon deficiency. Am J Physiol. 1979; 236(3):E263–E271.
【9】Cherrington AD, Liljenquist JE, Shulman GI, Williams PE, Lacy WW. Importance of hypoglycemia- induced glucose production during isolated glucagon deficiency. Am J Physiol. 1979; 236(3):E263–E271.
【10】Cherrington AD. Control of glucose production in vivo by insulin and glucagon,. In: Jefferson LS, Cherrington AD, Goodman HM, eds. The Handbook of Physiology: The Endocrine Pancreas and Metabolic Regulation. Vol. 2. New York, New York, USA: Oxford Press; 2001:759–785.
【11】Stevenson RW, Williams PE, Cherrington AD. Role of glucagon suppression on gluconeogenesis during insulin treatment of the conscious diabetic dog. Diabetologia. 1987;30(10):782–790.
【12】Davis MA, Williams PE, Cherrington AD. Effect of glucagon on hepatic lactate metabolism in the conscious dog. Am J Physiol. 1985;248(4 pt 1):E463–E470.
【13】Fradkin J, Shamoon H, Felig P, Sherwin RS. Evidence for an important role of changes in rather than absolute concentrations of glucagon in the regulation of glucose production in humans. J Clin Endocrinol Metab. 1980;50(4):698–703.
【14】Magnusson I, Rothman DL, Gerard DP, Katz LD, Shulman GI. Contribution of hepatic glycogenolysis to glucose production in humans in response to a physiological increase in plasma glucagon concentration. Diabetes. 1995;44(2):185–189.
【15】Muller MJ, Moring J, Seitz HJ. Regulation of hepatic glucose output by glucose in vivo. Metabolism. 1988;37(1):55–60.
【16】Nielsen MF, Wise S, Dinneen SF, Schwenk WF, Basu A, Rizza RA. Assessment of hepatic sensitivity to glucagon in NIDDM: use as a tool to estimate thecontribution of the indirect pathway to nocturnal glycogen synthesis. Diabetes. 1997;46(12):2007–2016.
【17】Wada M, Connolly CC, Tarumi C, Neal DW, Cherrington AD. Hepatic denervation does not significantly change the response of the liver to glucagon inconscious dogs. Am J Physiol. 1995; 268(2 pt 1):E194–E203.
【18】Dobbins RL, Davis SN, Neal DW, Cobelli C, Jaspan J, Cherrington AD. Compartmental modeling of glucagon kinetics in the conscious dog. Metabolism. 1995;44(4):452–459.
【19】Unger RH,Cherrington AD.Glucagonocentric restructuring of diabetes:a pathophysiologic and therapeutic makeover.J Clin Invest,2012,122:4-12.
【20】Liu Z,Kim W,Chen Z,et al.Insulin and glucagon regulate pancreatic alpha-cell proliferation.PLoS One,2011,6:e16096.
【21】Shah P,Vella A,Basu A,et al.Lack of suppression of glucagon contributes to postprandial hyperglycemia in subjects with type 2 diabetes mllitus.J Clin Endocrinal Metab,2000,85:4053-4059.
【22】Cryer PE.Hypoglycaemia:the limiting factor in the glycaemic management of type1and type2 diabetes.Diabetologia,2002,45:937-948.
【23】谷丽,张丽,胰岛α细胞在糖尿病发病及治疗领域中的研究进展,中国糖尿病杂志2017年2月第25卷第2期.
【24】郭航,常宝成,杨菊红,等.不同病程2型糖尿病患者胰岛α及β细胞功能评价,中华全科医师杂志,2013,12:874-878






