新发表《中国糖尿病肾脏病防治指南(2021年版)》
近日,《中华糖尿病杂志》和《国际内分泌代谢杂志》同步发表《中国糖尿病肾脏病防治指南(2021年版)》[1]。
一、流行病学
我国2型糖尿病(T2DM)患者的DKD 患病率为21.8%。
二、定义
糖尿病肾脏病(DKD)是指由DM所致的慢性肾脏病,主要包括尿白蛋白/肌酐比值(UACR)≥30mg/g和(或)估算的肾小球滤过率(eGFR)<60 ml·min?1·(1.73 m2)?1,且持续超过3 个月。
DKD是由慢性高血糖所致的肾损害,病变可累及全肾(包括肾小球、肾小管、肾间质及肾血管等),临床上以持续性白蛋白尿和(或)eGFR进行性下降为主要特征,可进展为ESRD。近年发现肾小管异常在DKD早期即可出现,并成为目前重要的治疗靶点。
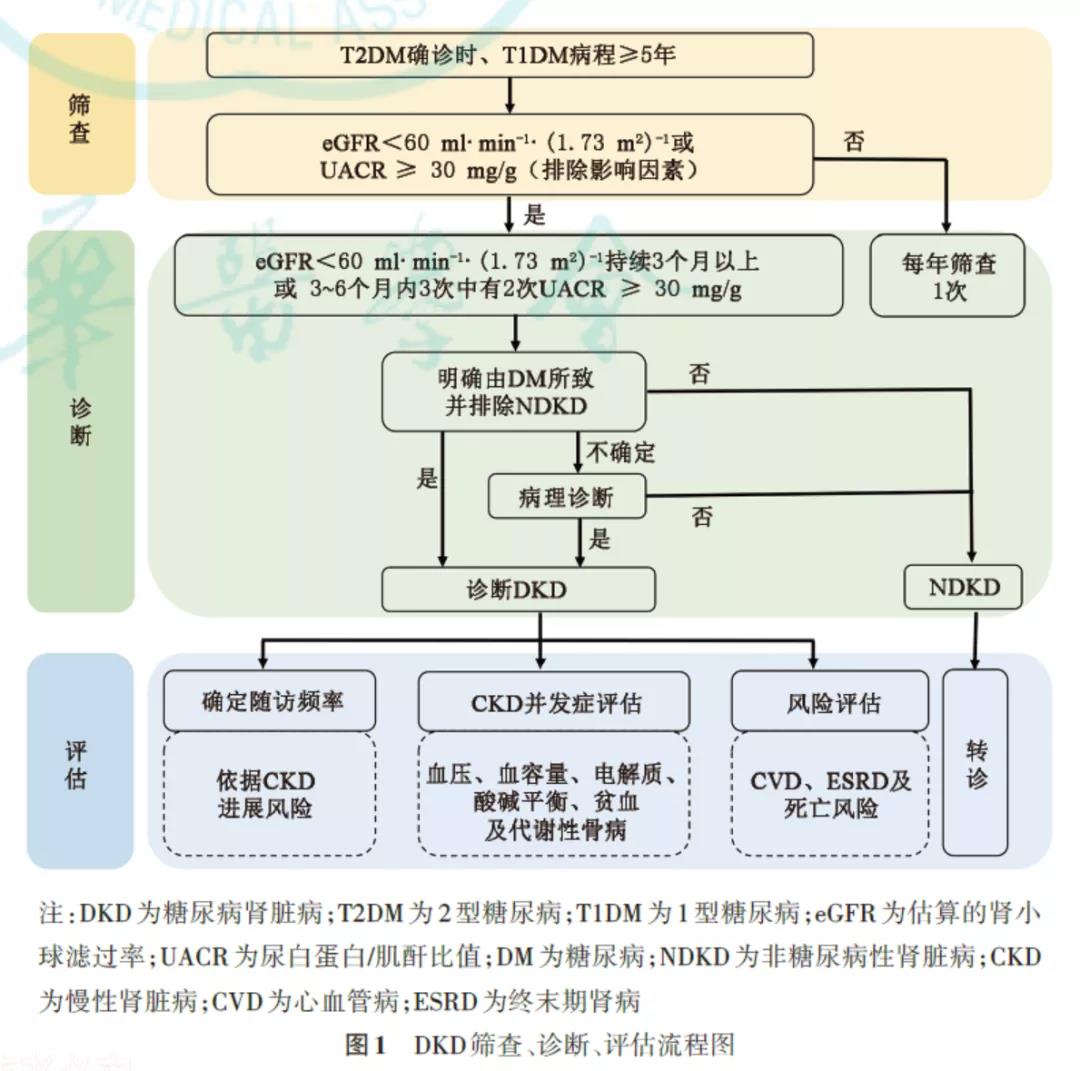
三、DKD 的筛查
1.筛查的人群与时机
推荐病程5年以上的1型糖尿病患者及T2DM患者在确诊时就应进行UACR 检测和eGFR 评估以早期发现DKD,以后每年应至少筛查1次。成本?效益分析显示,在新诊断的T2DM患者中进行DKD筛查可节省医疗费用。
2.筛查指标
1.尿白蛋白:推荐采用随机尿测定UACR反映尿白蛋白排泄情况。
2.eGFR:推荐≥18岁成人采用酶法检测血肌酐的CKD 流行病学合作研究(CKD ? EPI)公式计算eGFR。使用该公式计算的eGFR<60 ml·min?1·(1.73 m2)?1时,可称为eGFR下降。
3.其他指标:可测定肾小管损害标志物,如胱抑素C、β2微球蛋白、ɑ1?微球蛋白、视黄醇结合蛋白、中性粒细胞明胶酶相关脂质运载蛋白、肾损伤分子1等,注意排除影响因素,依据2~3次结果判定。采用彩色多普勒超声评估肾内血流动力学变化情况,同时排除尿路梗阻、肾动脉狭窄等其他疾病。
四、DKD诊断标准
目前DKD通常是根据持续存在的白蛋白尿和(或)eGFR下降、同时排除其他原因引起的CKD而做出的临床诊断。在明确DM作为肾损害的病因并排除其他原因引起CKD的情况下,至少具备下列一项者可诊断为DKD。
1.排除干扰因素的情况下,在3~6 个月内的3 次检测中至少2 次UACR≥30 mg/g 或UAER≥30mg/24h(≥20 μg/min)。
2.eGFR<60 ml·min?1·(1.73 m2)?1持续3 个月以上。
3.肾活检符合DKD的病理改变。
在临床诊断DKD时需要注意的问题:
(1)明确DM与CKD之间的因果关系:
典型的DKD临床表现包括:病程较长的DM、合并视网膜病变、出现白蛋白尿而无血尿,以及eGFR 逐渐下降等。
(2)正常白蛋白尿糖尿病肾脏病(NADKD):部分DKD 患者尽管eGFR 下降,但仍表现为正常白蛋白尿。
NADKD 在T1DM 合并DKD 的患者中占20%~60%,在T2DM 合并肾损害的患者中占10%~60%。我国的研究显示,T2DM 患者中NADKD 的患病率为25.47%,在高龄、女性及血糖控制良好的人群中更常见。
(3)糖尿病视网膜病变(DR):诊断DKD的重要依据之一,合并增殖期DR对于DKD的诊断更具特异性,但二者并非完全一致的关系,尤其是在T2DM患者中。研究发现,DR 进展与肾脏病理改变及ESRD 进展程度相关。T1DM合并DKD的患者常常合并DR,而DR并非诊断T2DM患者DKD的必备条件。
4.糖尿病合并NDKD:我国一项对505例T2DM合并非典型糖尿病肾损害的患者进行肾活检的研究显示,59.8% 诊断为DKD,34.5% 为NDKD,5.7%为DKD合并NDKD。
五、DKD的肾脏病理改变
DKD典型的肾小球病理改变包括肾小球基底膜增厚、系膜基质增宽及肾小球硬化。足细胞功能异常及凋亡在白蛋白尿的发生、发展中具有重要作用。
六、DKD的临床分期
在确诊DKD后,应根据GFR及尿白蛋白水平进一步判断CKD分期,同时评估DKD进展风险及明确复查频率。
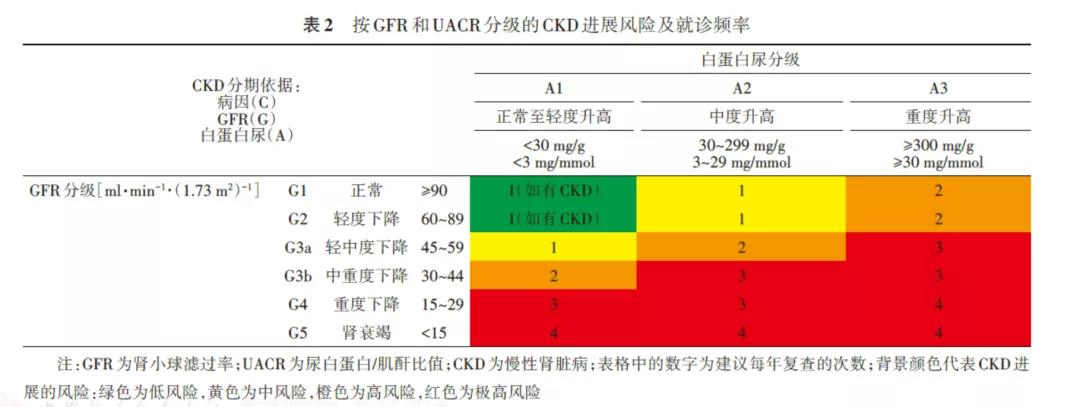
七、CKD并发症评估
当eGFR<60 ml·min?1·(1.73 m2)?1(CKD G3~5期)时更容易出现CKD并发症,包括血压升高、容量负荷过重、电解质紊乱、代谢性酸中毒、贫血及代谢性骨病等,并且随肾病进展而逐渐加重。
八、DKD的预后评估
1.心血管风险评估:DKD显著增加DM患者的CVD及其相关死亡风险,并且CVD是DKD患者致死的主要原因。我国一项对545例DM患者为期12年的随访研究提示,CVD是DKD患者死亡的首要原因(43.6%)。
2.ESRD风险评估:DKD是ESRD的主要原因,美国有30%~50%的ESRD由DM引起。1999 年北京血液透析患者中DKD 为病因者占9%,2011 年这一数字上升到35.1%。
3.死亡风险评估:DKD 患者的全因死亡风险随肾病进展而明显升高。我国的研究提示,DM 患者CKD 死亡风险是非DM 患者的13.1 倍。
九、DKD 的防治
1.一般治疗
(1)总热量:《中国2型糖尿病防治指南(2020年版)》推荐DM 患者每天能量摄入按25~30 kcal/kg计算,可根据体重、活动量、年龄、性别、应激情况再行调整。对于肥胖患者应相应减少热量摄入。
(2)蛋白质摄入:对于未进行透析治疗的DKD患者,推荐的蛋白质摄入量为0.8 g·kg?1·d?1;而透析患者常存在营养不良,可适当增加蛋白质摄入量至1.0~1.2 g·kg?1·d?1。
(3)钠、钾摄入:DKD患者每日的钠摄入量应低于2.3 g(约相当于6.0 g氯化钠的钠含量)。
2.生活方式
(1)戒烟:,吸烟是DM患者尿白蛋白进展和肾功能下降的独立危险因素,并增加CKD患者的CVD风险。随着吸烟量的增加,UACR水平和DKD患病率均显著增加。
2.运动:DKD患者应进行每周至少150 min(例如每周5次、每次30 min)的与心肺功能相匹配的运动。
3.体重控制及减重手术
有研究表明,超重或肥胖T2DM患者采用强化生活方式干预8 年,平均每年体重减轻8.6%,能显著降低其CKD风险31%。
十、血糖控制目标
1.血糖控制的评估指标
HbA1c联合自我血糖监测(SMBG)和持续葡萄糖监测(CGM)是临床上评估DKD患者血糖控制情况的重要方式,如果HbA1c已达标,但SMBG和CGM的结果显示血糖波动很大或提示低血糖,仍需调整治疗方案。葡萄糖目标范围内时间(TIR)是指24h中由SMBG 或CGM 记录的血糖在目标范围(3.9~10.0 mmol/L)的时间或占比,可更好地反映血糖波动情况。
2.血糖控制的目标
HbA1c<6%或>9%均会增加心血管及死亡风险,而强化降糖的肾脏保护作用需要较长时间(2~10年)才能出现。因此,在制定DKD患者的血糖控制目标时,应根据年龄、糖尿病病程、预期寿命、合并症、并发症、低血糖风险等,制定个体化控制目标。

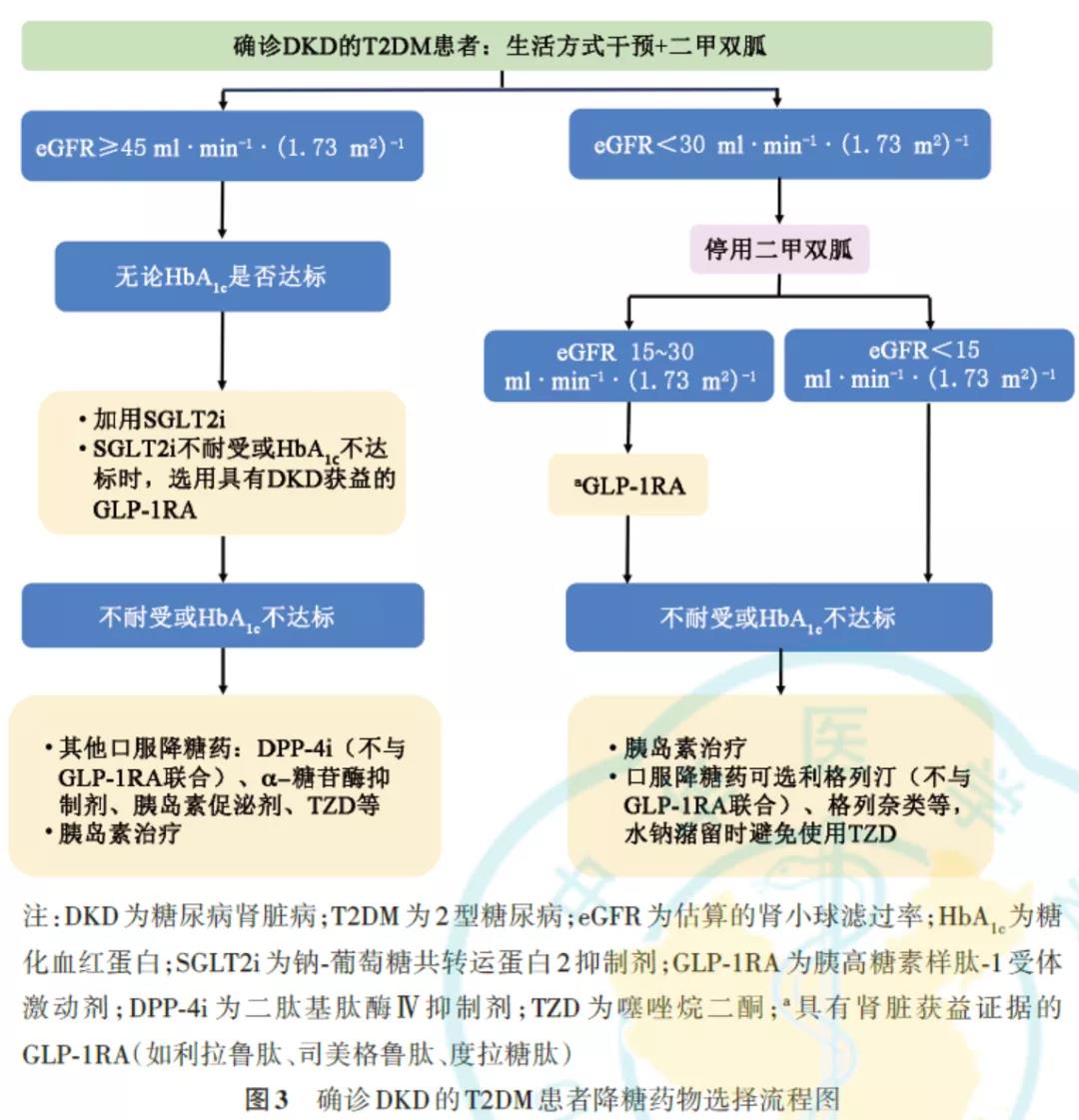
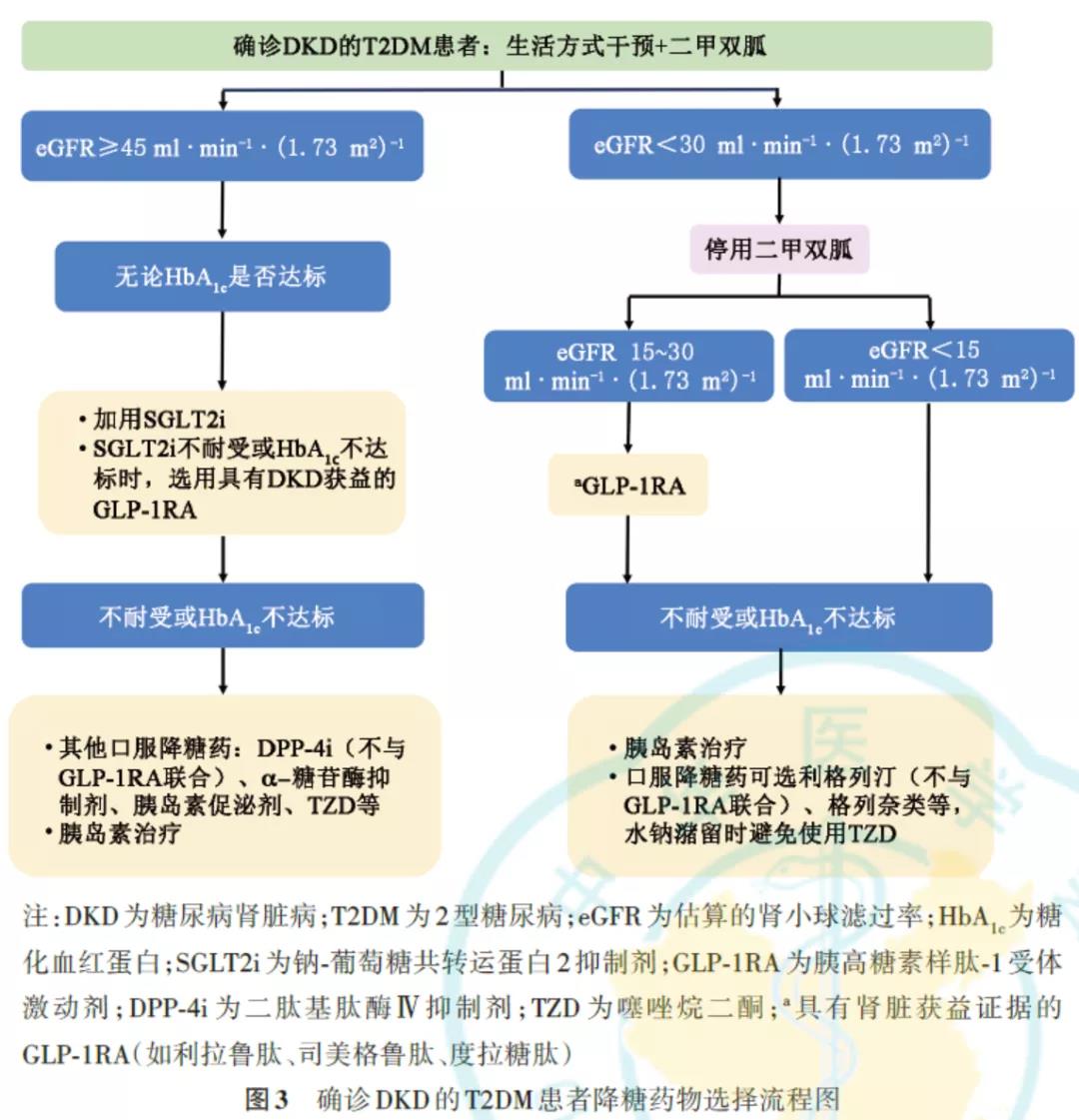
十一、调脂治疗
DKD患者更易合并脂质代谢紊乱。合理的血脂控制有助于降低DKD非透析患者的CVD及死亡风险,减少肾脏不良事件。
1.推荐低密度脂蛋白胆固醇(LDL?C)作为DKD患者血脂控制的主要目标,首选他汀类药物治疗。
2.推荐DKD患者的LDL?C目标值<2.6 mmol/L,其中动脉粥样硬化性心血管病(ASCVD)极高危患者的LDL?C应<1.8 mmol/L。DKD患者每年应至少检查1次血脂,起始降脂药物治疗者应1~3个月后复查,之后每3~12个月复查。
十二、可能延缓尿白蛋白进展的其他治疗措施
微循环障碍、纤维蛋白原升高、血小板聚集、炎症及氧化应激等均可促进尿白蛋白进展。
十三、中医中药
十四、避免肾损伤的药物
目前临床常见的肾毒性药物包括某些抗生素(氨基糖苷类、青霉素类、头孢菌素类、两性霉素B、抗结核类、磺胺类药物等)、非甾体类抗炎药、抗肿瘤药物、对比剂、某些中草药(马兜铃酸、木通等)。
参考文献:
1.中华医学会糖尿病学分会微血管并发症学组. 中国糖尿病肾脏病防治指南(2021年版)[J]. 中华糖尿病杂志, 2021, 13(8): 762-784. DOI: 10.3760/cma.j.cn115791-20210706-00369.






